2026.4.13
本文提出PASTA框架,利用条件扩散模型和增强的病理意识实现MRI到PET的跨模态图像转换,有效保留结构和病理细节,并通过循环交换一致性及2.5D体素生成策略,显著提升阿尔茨海默病诊断精度,其合成PET图像性能接近真实PET。
Title题目
01
Translating MRI to PET through conditional diffusion models with enhanced pathology awareness
通过条件扩散模型实现增强病理意识的MRI到PET转换
文献速递介绍
02
阿尔茨海默病(AD)是一种进行性神经退行性疾病,早期检测对其治疗至关重要。诊断AD需多学科工具,包括提供解剖信息的MRI和测量葡萄糖代谢的PET。PET能敏感捕捉功能异常,在AD早期诊断中被认为更准确,但高成本和辐射限制了其广泛应用。MRI更普及且无创,但诊断敏感性较低。将MRI数据转换为合成PET有望弥补这一空白。然而,当前基于生成模型(特别是扩散模型)的跨模态医学图像转换方法,主要侧重结构完整性,常忽视病理特征的准确保留。PASTA旨在解决这一关键挑战,提出一个端到端基于扩散模型的框架,实现具有临床意义的MRI到PET体素级转换,并增强对病理的感知。
Aastract摘要
03
正电子发射断层扫描(PET)因其对神经退行性疾病诊断提供关键功能洞察而被广泛认可,但其高成本和辐射暴露限制了普及。相比之下,磁共振成像(MRI)无这些限制,但在诊断敏感性上低于PET。为克服此局限,通过MRI生成合成PET成为可行方案。现有生成模型在跨模态医学图像转换中多强调结构保留而忽略病理意识。本文提出PASTA,一个基于条件扩散模型的图像转换框架,具备增强的病理意识。PASTA通过高度交互的双臂架构和多模态条件整合,在保留结构和病理细节方面超越了现有最先进方法。此外,引入的新型循环交换一致性策略和体素生成策略显著提升了PASTA生成高质量3D PET图像的能力。定性和定量结果表明,合成PET图像质量高且具有病理意识,在阿尔茨海默病诊断中,其性能较MRI提升4%,几乎达到真实PET水平。
Method方法
04
本文提出PASTA框架,采用条件去噪扩散概率模型(DDPM)实现3D脑部MRI到PET的病理感知转换。PASTA具有对称双臂架构,包含一个调节器臂和一个去噪器臂,并通过自适应条件模块(AdaGN)整合多模态条件。调节器臂处理MRI输入并生成多尺度任务特定表示。去噪器臂则在时间步、临床数据和任务特定表示等多种条件下,从噪声中逐步恢复干净的PET图像。为增强病理意识,PASTA将MetaROIs作为病理先验,通过损失权重图强调关键的代谢低下区域。此外,引入循环交换一致性(CycleEx)训练策略,在不增加额外学习参数的前提下,通过循环翻译增强双臂间的信息共享,提升生成质量。最后,采用2.5D体素生成策略,通过输入N个连续邻近切片,并在训练后对重叠切片进行加权平均,有效平衡训练效率和3D PET生成的一致性,缓解2D网络可能导致的切片不一致问题。
Discussion讨论
04
PASTA的出色性能源于其高度交互的双臂架构、多模态条件整合、循环交换一致性以及2.5D体素生成策略。这些创新设计确保了生成的PET图像不仅在结构上忠实于MRI,更能准确反映病理变化,从而在临床诊断中具有实际意义。通过融合MRI结构信息、临床数据(如认知评分、遗传风险因子)和MetaROIs病理先验,模型显著增强了对疾病相关变化的敏感性。MetaROIs引导模型聚焦AD关键代谢低下区域,而CycleEx则促进了双臂间任务特定特征的提取与信息共享。尽管本研究有力地证明了PASTA在AD诊断中的巨大潜力,但目前缺乏正式的临床阅片研究来定量评估合成PET的实际诊断效用,这是未来工作需要进一步解决的局限。
Conclusion结论
05
本文提出了PASTA框架,一个利用条件扩散模型实现脑MRI到PET转换的新颖方法。PASTA通过其高度交互的双臂架构和多模态条件作用,在目标模态中出色地保留了结构和病理模式。CycleEx和体素生成策略进一步提升了其生成高质量3D PET扫描的能力。全面的消融研究证实了这些关键设计的有效性。在AD诊断中,PASTA实现了比MRI更高的诊断准确率,并且AUC甚至超过了真实PET扫描。其独特的病理意识可能源于多模态条件和病理先验的有效整合,以及关键组件之间的协同作用。PASTA在连接结构和功能性脑退化过程方面展现出巨大潜力,为临床应用提供了有前景的进展。
Results结果
06
定性结果显示,PASTA生成的PET扫描在保真度和病理细节方面优于现有最先进方法,尤其能准确捕获AD患者颞顶叶的代谢降低等关键病理特征。临床专家评估认为,生成的PET图像真实且与实际PET相当,尽管更平滑,但对临床诊断无碍,且对AD诊断的病理敏感性高于MRI。定量评估表明,PASTA在ADNI和内部数据集上的MAE、MSE最低,PSNR和SSIM最高,且统计学意义显著。在AD诊断分类任务中,PASTA合成PET图像的诊断准确率较MRI提高超过4%,AUC达到91.63%,接近真实PET性能。病理区域局部评估进一步证实,PASTA在疾病相关MetaROIs区域的生成保真度更高。敏感性分析显示ADAS和MMSE是影响生成结果的最关键临床变量。Neurostat 3D-SSP Z值图也验证了PASTA在病理意识方面的优势。消融研究确认了CycleEx、病理先验和临床数据整合等关键设计的有效性,其中CycleEx对生成质量影响最大。对输入邻近切片数量的消融实验表明N=15是最佳设置。公平性评估显示PASTA在不同年龄、性别和诊断组之间表现出一致的准确性,无显著偏差。
Figure图
07
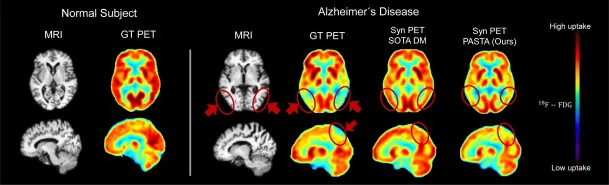
图1.针对阿尔茨海默病,PET显示颞顶叶(底部圆圈)葡萄糖摄取明显减少,以更高的敏感性反映了MRI上的萎缩。与真实PET(GT)相比,最先进的扩散模型(SOTA DM)未能从MRI输入中恢复合成PET(Syn)中的此类病理。相比之下,PASTA在保留疾病特异性病理方面显示出改进。
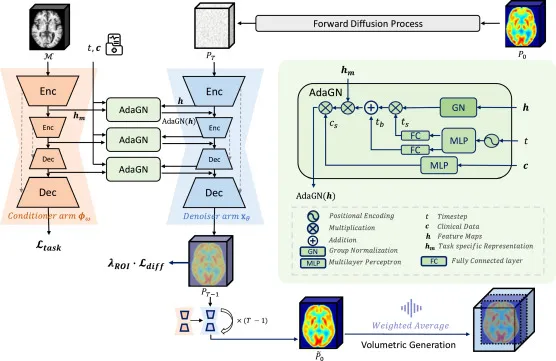
图2.PASTA具有对称的双臂结构,包括一个调节器臂(ϕω)、一个去噪器臂(xθ)和自适应条件模块(AdaGN)。通过AdaGN,PASTA根据时间步t、临床数据c和来自ϕω的任务表示hm对xθ的特征图h进行条件化。它通过体素生成策略实现高质量的3D PET合成。
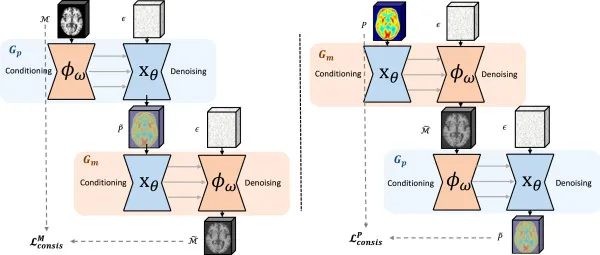
图3.PASTA的循环交换一致性(CycleEx)策略。两个转换映射Gp:M→P和Gm😛→M保持循环一致性。此外,它们的网络架构是镜像的:两者都包含相同的调节器臂ϕω和去噪器臂xθ,但位置互换。该策略确保了两个臂之间的信息共享。
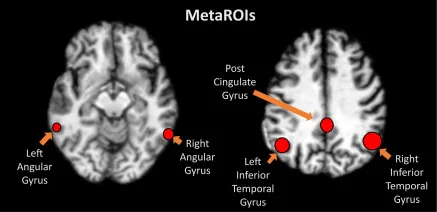
图4.脑部MRI上的MetaROIs示意图。

图5.跨模态合成方法的定性比较。第一行显示了无明显病理的正常对照受试者的图像,第二行显示了颞顶叶(左下和右下部分)有明显代谢减低的AD患者。第三行放大了左侧颞顶叶。对于正常受试者,大多数基线方法能很好地恢复结构和代谢信息;对于AD受试者,PASTA表现出卓越的生成保真度和病理保留能力。
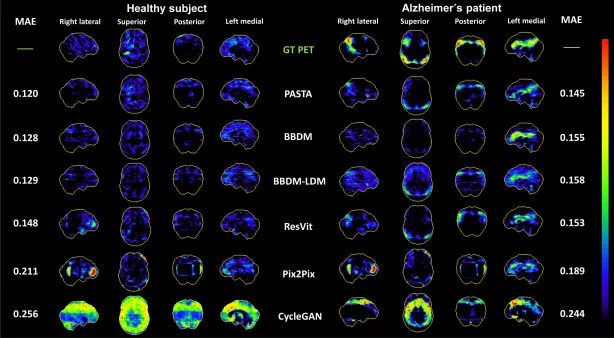
图6.Neurostat 3D-SSP为健康受试者(左)和阿尔茨海默病患者(右)生成的Z值图。我们展示了真实(GT)PET和各种方法合成PET扫描在不同大脑皮层区域的全局代谢Z值图。合成PET图与GT图之间的平均绝对误差(MAE)并列显示。
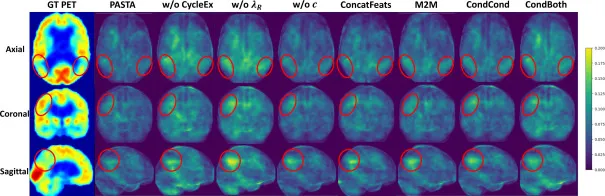
图7.PASTA关键设计消融研究的误差图,针对一名AD诊断受试者。我们分别展示了其真实(GT)PET以及沿三个方向扫描的平均误差图。具体来说,我们用红色圆圈标记了受AD高度影响的区域。
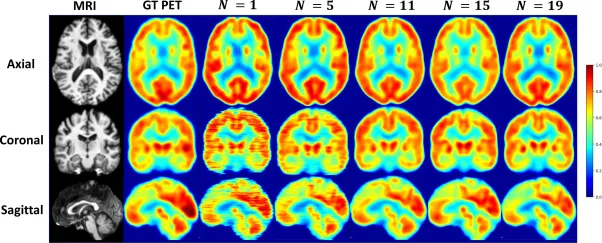
图8.输入邻近切片数量N的消融研究。我们展示了在三种方向(轴位、冠状位和矢状位)上,不同N值下合成的PET扫描图,其中轴位切片作为网络的输入。

图9.输入切片方向的消融研究以及来自三个方向的合成扫描的平均值。输入切片方向对合成PET扫描的影响最小。