2026.4.3
本文提出ACE-ProtoNet,一个统一的冠状动脉分割框架,通过结合部分冻结的视觉基础模型和可训练的CNN双编码器、基于协方差和特征值分析的自适应特征门(ACE-Gate)以及不确定性感知原型学习头(UPL-Head),有效整合异构特征并利用预测不确定性,实现了对复杂血管结构的高精度、鲁棒性及泛化能力强的分割。
Title题目
01
ACE-ProtoNet: Adaptive covariance eigen-gate and uncertainty-aware prototype learning for coronary artery segmentation
ACE-ProtoNet: 基于自适应协方差特征门和不确定性感知原型学习的冠状动脉分割
文献速递介绍
02
冠心病是全球主要的死亡原因,精确诊断至关重要。冠状动脉CT血管造影(CCTA)是主要的无创成像方式,但其自动分割面临诸多挑战:血管与背景对比度低、患者间解剖结构变异大以及血管树形拓扑复杂且边界模糊。现有深度学习方法,如CNN受限于有效感受野,Transformer模型缺乏局部归纳偏置,而基于视觉基础模型(VFM)的混合架构通常采用简单或启发式融合策略,且忽视了3D切片间的连续性和特征统计异构性。此外,在钙化区域或远端血管等模糊区域,预测不确定性问题未被充分探索。为解决这些问题,本文提出ACE-ProtoNet,一个结合自适应协方差特征门(ACE-Gate)和不确定性感知原型学习头(UPL-Head)的统一框架。该框架采用部分冻结的SAM-Med3D作为3D基础模型驱动编码器,并结合3D U-Net CNN形貌编码器,通过ACE-Gate实现统计学原理的异构特征融合,并通过UPL-Head利用不确定性指导原型学习,以增强对模糊区域的鲁棒性。
Aastract摘要
03
从冠状动脉CT血管造影(CCTA)图像中准确分割冠状动脉对于定量狭窄评估、斑块特征分析和手术规划至关重要。然而,血管与背景对比度低、解剖变异性大以及复杂树状血管形态给自动化分割带来了巨大挑战。为解决这些问题,我们提出了ACE-ProtoNet,一个统一的框架,它结合了自适应协方差特征门(ACE-Gate)和不确定性感知原型学习头(UPL-Head),以实现稳健准确的冠状动脉分割。该架构基于一个并行的双编码器骨干网络,该网络协同作用于一个部分冻结的视觉基础模型(VFM)以进行全局结构编码,以及一个可训练的CNN以进行局部细粒度特征提取。为了协调这些异构特征流,ACE-Gate通过协方差分析和特征值分解明确建模通道间依赖关系,产生基于统计学原理的通道级门控以实现特征集成。同时,UPL-Head利用体素级预测不确定性来调节原型引导的注意力并动态更新原型,从而增强难以分类区域的表示鲁棒性并提高整体分割精度。在两个内部数据集和四个公共数据集上进行的大量实验表明,ACE-ProtoNet在多项指标上始终优于十二种最先进的方法,展现出卓越的跨领域泛化能力以及强大的跨模态和跨解剖结构迁移能力。
Method方法
04
ACE-ProtoNet框架包含双编码器骨干网络、ACE-Gate模块、解码器和UPL-Head。双编码器将部分冻结的SAM-Med3D模型(仅微调最后两个ViT块)用于全局结构编码,同时使用可训练的3D U-Net风格CNN编码器提取局部细粒度特征。ACE-Gate通过协方差估计和特征值分解(EVD)来推导方差指标,生成自适应门控机制,从而实现异构特征的统计学原理融合。具体而言,它将VFM和CNN特征投影到统一空间,计算通道间协方差矩阵,然后对协方差矩阵进行EVD以提取特征值作为全局特征方差的紧凑描述符。一个轻量级MLP将这些特征值映射到通道级重要性权重,用于动态平衡VFM和CNN特征,生成最终融合输出。解码器通过跳跃连接从CNN编码器逐步上采样融合特征,以恢复高分辨率细节。UPL-Head通过三个互联组件细化预测:首先,使用香农熵通过辅助分割头计算体素级不确定性图。其次,在不确定性感知原型引导预测中,体素特征作为查询,原型作为键/值,通过注意力机制生成原型精炼特征,并由不确定性图进行调制(X̃' = X̃ ⊗ (1+U)),以在模糊区域加强全局类别先验。同时,计算显式体素-原型相似度图,然后与不确定性调制特征拼接,通过3D卷积和Sigmoid激活生成最终分割概率图。最后,在在线不确定性感知原型学习中,体素特征被分配到其最近的原型,并通过不确定性加权平均进行聚合,实现软难样本挖掘,更新原型以更具代表性,尤其是在复杂血管拓扑中。总损失函数结合了分割损失(加权交叉熵和Dice损失)和体素-原型对比损失,以优化体素级准确性和判别性嵌入空间。
Discussion讨论
04
本研究进一步探讨了ACE-ProtoNet的优越性,特别是在泛化能力和可迁移性方面。在对未知域的泛化能力评估中,ACE-ProtoNet在CTA119与ASOCA及ImageCAS之间的所有四个跨域场景中,始终优于六种竞争方法,例如在CTA119→ASOCA设置中DSC达到84.86%,比次优方法Ensembled-SAMs高出1.99%。定性结果显示,ACE-ProtoNet在域偏移下仍能有效保持主要动脉的连接性并重建解剖学上忠实的血管结构,尽管在一些细小远端分支可能存在少量欠分割。这种强大的泛化能力得益于其架构设计,使其适用于实际CAD应用。在跨解剖结构和跨模态的可迁移性评估中,ACE-ProtoNet在腹部CT的门静脉系统分割(PVS203)、MRA的脑血管分割(MIDAS)以及胸部CT的肺气道分割(ATM22)任务中均表现出色,DSC分别达到92.55%、72.50%和93.23%,持续优于SOTA方法。这些结果表明,ACE-ProtoNet不仅是冠状动脉分割的专用解决方案,更是一个鲁棒且通用的架构,能够通过统计学原理特征门控和不确定性引导的表示学习,适应多样化的解剖配置和成像模态。尽管ACE-ProtoNet取得了最先进的性能和强大的泛化能力,其主要局限性在于在某些情况下可能产生拓扑不完整的分割,例如血管不连续。目前的框架缺乏对这些结构不连续性进行事后校正的专门机制。未来的研究将集中于显式的拓扑修复,可能采用多阶段细化策略,如基于中心线的阶段来连接碎片化血管,然后使用隐式神经表示模块来重建连续的腔内几何结构。此外,计划整合基于图的推理,将断开的血管碎片建模为图节点,使图卷积网络学习它们的空间和形态关系,从而为识别解剖学一致的重连提供高级指导。通过将这些结构感知修复技术与当前的分割框架结合,目标是显著提高拓扑完整性,以实现更可靠的冠状动脉提取。
Conclusion结论
05
本文提出了ACE-ProtoNet,一个旨在克服冠状动脉分割中准确性、鲁棒性和泛化性长期挑战的统一框架。该框架整合了三个协同创新的组件:(1)一个并行的双编码器骨干网络,结合了部分冻结的视觉基础模型提供的全局结构表示和可训练CNN捕获的细粒度局部细节;(2)ACE-Gate,通过协方差和特征值分析执行统计学原理的特征融合;(3)UPL-Head,利用预测不确定性指导原型适应并增强模糊血管区域的可靠性。在两个内部数据集和三个公共数据集上进行的大量实验证明了ACE-ProtoNet卓越的准确性和泛化能力,在描绘细小远端血管和在域偏移下保持鲁棒性方面具有显著优势。消融研究证实了双编码器、ACE-Gate和UPL-Head的有效性,而跨解剖结构迁移实验进一步证明了该框架对门静脉和脑血管等其他血管结构的适应性。未来的工作将侧重于显式的拓扑修复,可能整合基于图的推理以识别血管不连续性,并采用多阶段几何细化以确保血管连续性。通过将基础模型表示与统计学原理的融合和不确定性引导的原型学习相结合,ACE-ProtoNet为自动化冠状动脉分割建立了一个统计学指导和临床依据的范式,为更可靠的定量分析和心血管成像决策支持铺平了道路。
Results结果
06
在CTA119、ASOCA和ImageCAS三个基准数据集上的量化结果显示,ACE-ProtoNet在所有六项评估指标(DSC、SE、ASSD、clDice、SR、SP)上均持续优于十二种最先进的方法。在CTA119数据集上,ACE-ProtoNet的DSC为87.34%,比最佳CNN模型和最佳血管特异性方法分别高出2.76%和2.24%。在公共ASOCA和大型ImageCAS数据集上,它也保持了领先性能,DSC分别为90.18%和86.73%,ASSD最低,clDice最高,SR和SP表现优异,显著减少了血管碎片化。所有性能提升均具有统计学意义(p<0.01)。定性结果(3D渲染和2D切片)进一步证实了ACE-ProtoNet能够提供连续且解剖学一致的3D重建,精确描绘细小血管和复杂分叉,避免了现有方法的碎片化和细节丢失问题。计算复杂度分析表明,ACE-ProtoNet参数量和计算成本适中,推理时间为每体积22.4秒,具有实际临床应用可行性。消融实验验证了双编码器、ACE-Gate和UPL-Head各组件的有效性及其协同作用。双编码器整合VFM和CNN特征可带来显著性能提升。ACE-Gate进一步提升了性能,并使激活图更清晰、更局部化。UPL-Head作为关键细化模块,持续提升分割质量。体素-原型对比损失权重β设为0.2时效果最佳,平衡了特征可区分性和体素级精度。每个类别原型数量K设为3时达到最佳性能,表明模型对该超参数具有鲁棒性,且较少原型即可有效捕捉血管内类变异。
Figure图
07

图1. 准确识别椎体压缩
冠状动脉CCTA分割的挑战。(a, c)CCTA扫描的代表性轴位切片,(b, d)显示了方框区域的放大视图,以突出冠状动脉的低对比度和模糊边界(红色为真实值)。(e)强度直方图显示冠状动脉(红色)和周围组织(青色)之间存在显著重叠,定量证明了血管与背景的低对比度。(f-i)四种不同患者情况的3D渲染,突出了显著的患者间解剖变异性和复杂的血管拓扑结构。(j, k)基线方法分割错误的示例,显示正确分割(红色)、过度分割(橙色)和欠分割(蓝色)区域,导致碎片化和连续性丢失。
性骨折的主要挑战。图1展示了两种异常骨折(轻度/重度)病变区域及其在不同模态中相邻正常椎体的比较。(a)、(b)分别是胸部正位X光片及其放大视图;©、(d)分别是胸部侧位X光片及其放大视图。箭头指示T12椎体的病变区域。
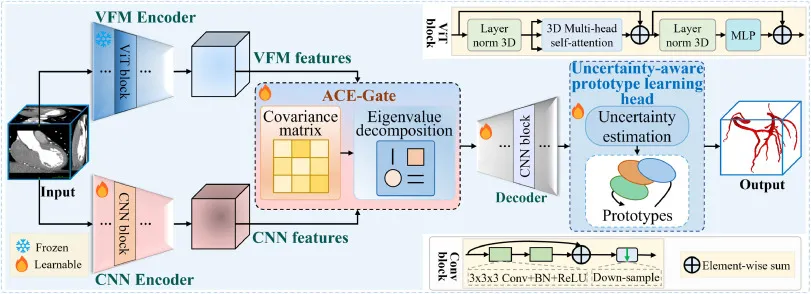
图2. 所提出的ACE-ProtoNet的整体架构。模型通过并行双编码器骨干处理输入的3D CCTA体数据。上层分支采用部分冻结的VFM编码器捕获全局结构表示,而下层分支使用完全可训练的CNN编码器提取细粒度、任务特定的局部特征。为协调这种异构性,提出的ACE-Gate通过协方差分析和特征值分解建模通道间依赖关系,提供了一种原则性的融合机制。融合后的特征随后由UPL-Head解码和细化,UPL-Head利用预测不确定性和类别级原型来增强分割精度。
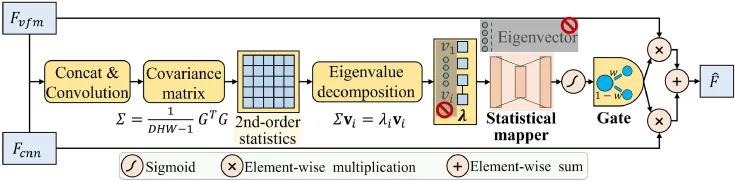
图3.ACE-Gate的结构。该机制在三个统计学基础阶段运行:(1)共同空间投影和统计建模:输入特征投影到统一空间,计算通道间协方差矩阵以捕获二阶统计信息(全局方差结构)。(2)特征值引导权重生成:特征值分解提取全局方差分布(λ)。统计映射器(MLP)将这些特征值映射为通道级重要性权重(w),弥合了全局统计结构和通道级融合相关性之间的差距。(3)通道级自适应融合:这些权重协调互补门控机制(w和1-w),动态平衡VFM衍生的全局语义和CNN基的局部细节,生成最终融合输出F̂。

图4.UPL-Head的结构。(1)不确定性估计(左上):一个辅助头通过香农熵计算体素级不确定性图(U)以识别模糊区域。(2)不确定性感知原型引导预测(左下):解码器特征通过注意力机制进行细化,其中体素作为查询,原型作为键/值。生成的特征(X̃)由不确定性进行调制(X̃' = X̃ ⊗ (1+U)),以放大全局先验。同时,计算显式相似度图(S)。这些被连接起来并通过一个带有Sigmoid的3D卷积产生最终分割(Pf)。(3)在线不确定性感知原型学习(右,仅训练):体素被分配到最近的原型(k*),并通过不确定性加权平均(执行软硬样本挖掘)进行聚合。这有效地优先处理“硬样本”(高不确定性)以增强原型可区分性,随后进行EMA更新。在推理期间,原型库是固定的。
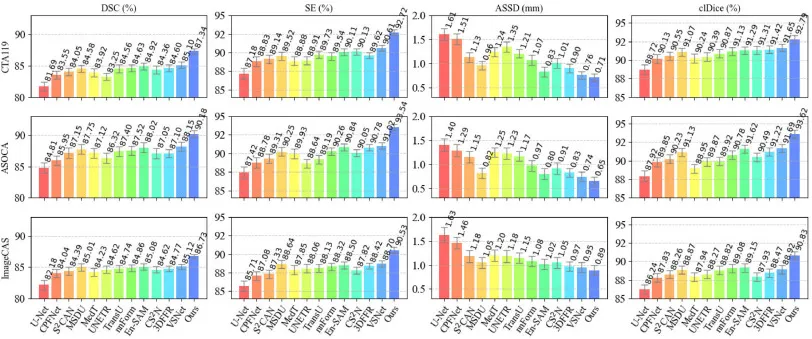
图5.不同方法的整体性能比较。量化结果在CTA119、ASOCA和ImageCAS数据集上以DSC (%)、SE (%)、ASSD (mm)和clDice (%)进行报告。DSC、SE和clDice值越高,ASSD值越低表示分割性能越好。图中方法名称已缩写。

图6.四个代表性病例的3D冠状动脉分割结果的定性比较。虚线圈突出显示了竞争方法表现出显著欠分割或过分割的区域,导致次优的分割结果。

图7.一个挑战性病例的详细2D和3D定性比较,每个面板下方报告了病例特定的DSC得分。每个子图显示了最终的3D渲染以及相应的多平面(轴位、冠状位、矢状位)2D视图,其中分割结果叠加在原始CT图像上。突出了两个挑战性感兴趣区域:细小的远端血管(箭头①,黄色框)和复杂的分叉(箭头②,蓝色框)。
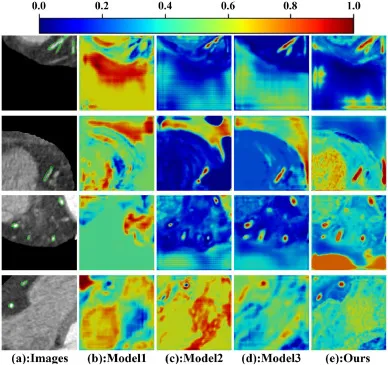
图8.通过特征激活图对模型组件进行视觉消融研究。列显示:(a)带有真实值(绿色)的原始图像;(b)基线(Model1);(c)Model1 + VFM(使用Sum融合,Model2);(d)Model1 + VFM + ACE-Gate(Model3);(e)带有UPL-Head的完整模型(Ours)。编码器最后一层的热图表示模型注意力(颜色越暖表示注意力越高)。从(b)到(e)激活图的逐渐锐化从视觉上证实了每个添加组件的功效及其在最终模型中的协同作用。

图9雷达图比较了所提出的方法与六种最先进方法在CCTA119数据集与ASOCA和ImageCAS数据集之间场景的跨域泛化性能。图表显示了DSC、SE、ASSD和clDice在四种训练-测试场景下的结果。我们的方法(Ours,粗红色线)实现了最佳性能,表现为前三个指标的面积最大,ASSD的面积最小。

图10CCTA119数据集与ASOCA和ImageCAS数据集之间在四种训练-测试配置下的跨域验证结果。在CTA119→ASOCA设置中,(A)表示在CTA119上训练并在ASOCA上测试,而(B)表示在ASOCA上进行域内训练和测试。类似的配置适用于ASOCA→CTA119(C-D)、CTA119→ImageCAS(E-F)和ImageCAS→CTA119(G-H)。每个病例的DSC、ASSD和clDice均有报告(DSC/clDice值越高,ASSD值越低表示性能越好)。正确分割区域显示为红色,欠分割为蓝色,过分割为黄色
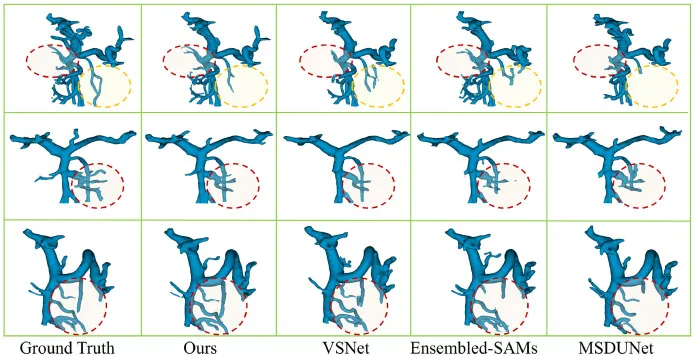
图11PVS203数据集上血管分割结果的3D可视化。虚线圈表示竞争方法可能存在欠分割或过分割的感兴趣区域。
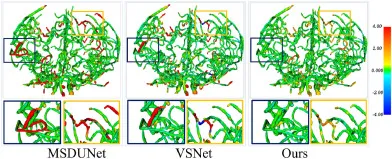
图12IDAS数据集上血管分割结果的3D可视化。颜色条表示预测表面与真实标注之间的带符号距离场。暖色(红色)表示正误差(过度分割),冷色(蓝色)表示负误差(欠分割)。