2026.3.2
本文提出了一种基于递归可变形扩散模型(RDDM)的鲁棒无接触动态胸腔肿瘤定位非刚性配准框架,该框架通过少量CT扫描重建4DCT序列,并利用广义迭代最近点(GICP)算法实现实时图像-患者配准,从而在减少辐射暴露的同时,实现对肿瘤的精确跟踪。
Title题目
01
Robust non-rigid image-to-patient registration for contactless dynamic thoracic tumor localization using recursive deformable diffusion models
基于递归可变形扩散模型的无接触动态胸腔肿瘤定位鲁棒非刚性图像-患者配准
文献速递介绍
02
肺癌肿瘤,特别是胸腔区域的肿瘤,由于呼吸运动,其精确的定位和跟踪面临挑战,可能导致靶向不准确、创伤增加和并发症。传统方法如术中低剂量CT、术前4DCT、电磁导航和超声成像均存在局限性,如辐射暴露高、分辨率低或侵入性强。当前研究主要关注如何获取精确反映病灶位置的影像数据,以及如何将这些数据与术中患者坐标系对齐以实现实时导航。本文提出一种鲁棒的无接触非刚性图像-患者配准框架,通过高效的递归可变形扩散模型(RDDM)从少量CT扫描生成完整的4DCT序列,并结合基于GICP的无接触实时配准算法,以实现精确的肿瘤定位和运动预测,减少辐射暴露,提高手术安全性和有效性。
Aastract摘要
02
可变形图像-患者配准在手术导航和医学成像中至关重要,但跨模态实时计算空间变换仍是主要临床挑战,常耗时、易出错且可能增加创伤或辐射暴露。现有方法在胸腔应用中受限于呼吸等生理运动。为解决此问题,本文提出了一种鲁棒、无接触的非刚性配准框架,用于动态胸腔肿瘤定位。该框架训练高效的递归可变形扩散模型(RDDM),仅通过吸气末和呼气末两次低剂量CT扫描,即可重建完整的4DCT序列,捕捉反映术中状态的呼吸动态。对于实时患者对齐,引入基于广义迭代最近点(GICP)的无接触非刚性配准算法,利用立体RGB-D图像捕获的患者皮肤表面点云,并通过融入法向量和膨胀-收缩约束增强鲁棒性并避免局部最小值。该框架在公开数据集和志愿者试验中得到验证,定量评估显示RDDM在不同呼吸相具有解剖保真度,PSNR达到34.01 ± 2.78 dB。此外,初步开发了基于4DCT的配准和手术导航模块以支持肿瘤定位和高精度跟踪。实验结果表明,该框架初步满足临床要求,并有望集成到下游手术系统中。
Method方法
03
该框架包含术前和术中两个阶段。术前阶段,训练好的RDDM网络利用吸气末和呼气末两相低剂量CT序列,迭代生成中间CT体数据,重建完整的4DCT数据集,并提取皮肤、肺部和肿瘤的动态4D形状信息。RDDM通过双分支扩散建模架构(DDPM-Ex和DDPM-In)捕捉呼吸运动的准对称性,实现从呼气到吸气和吸气到呼气的双向时间图像生成,确保解剖一致性和时间连贯性。术中阶段,使用立体RGB-D相机实时捕获胸部表面点云。采用鲁棒的基于GICP的点云配准方法,结合皮肤表面点云的法向量角度容差和膨胀-收缩阈值,实现生成的4DCT图像与术中患者解剖结构的实时对齐,并通过光学跟踪系统进行共同配准以评估精度。
Discussion讨论
04
本文提出的框架相较于传统术中肿瘤定位方法,显著减少了侵入性和辐射暴露,并通过持续估计皮下肿瘤位置和形态,提高了微创胸腔手术的准确性。扩散模型能够学习连续的呼吸运动模式,生成平滑的运动轨迹,有效避免了传统方法中常见的滑动和折叠伪影。与GAN/VAE模型不同,扩散模型能自然生成特定呼吸状态下的样本,准确反映呼吸周期中的位置变化。RDDM通过双向训练和融合机制,增强了中间帧的重建一致性和鲁棒性。为解决术中LDCT-患者配准中呼吸运动不匹配导致的定位误差,本研究进一步提出了4DCT-患者配准方法。该框架可部署在标准笔记本电脑上,更新速率超过10Hz。局限性包括训练和测试数据集的限制,以及RGB-D相机可能影响配准精度和刷新率。
Conclusion结论
05
本研究提出了一个用于动态胸腔肿瘤定位的新型无接触配准框架。该框架利用递归可变形扩散模型(RDDM)仅从两个低剂量CT相生成解剖学上一致的4DCT序列,并采用鲁棒的非刚性图像-患者配准策略,将合成的4DCT数据与术中患者解剖结构对齐,实现实时肿瘤定位和形态跟踪。实验结果表明,该模型在各种呼吸相下均能保持解剖准确性,SSIM达到0.92 ± 0.03,PSNR达到34.01 ± 2.78 dB,平均肿瘤定位误差为1.89 ± 0.73 mm,验证了其在跟踪结节轨迹和预测非刚性变形方面的精确性和鲁棒性。该RDDM模型具有可扩展性,适用于广泛的临床场景,为计算机辅助和机器人辅助胸腔手术提供了可扩展且辐射高效的解决方案。
Results结果
06
RDDM网络在公共4DCT数据集上进行训练和验证,从吸气末和呼气末CT图像生成中间呼吸相的4DCT序列。定性结果显示,生成的4DCT序列和变形场能有效捕捉呼吸期间的扩张和收缩趋势,并保持关键解剖特征的平滑过渡和一致表示。定量评估显示,生成的图像具有高保真度,平均PSNR为34.01 ± 2.78 dB,SSIM为0.92 ± 0.03,NMSE为0.00999 ± 0.00365。与现有方法相比,RDDM在生成质量和时间效率上表现优异。配准精度评估在模拟患者数据和志愿者数据上进行,在模拟数据上FRE为0.56 ± 0.23mm,在志愿者数据上平均FRE为1.36 ± 0.48mm,平均肿瘤定位误差(TPE)为1.89 ± 0.73mm,显示了该框架在实际应用中的可行性。
Figure图
07
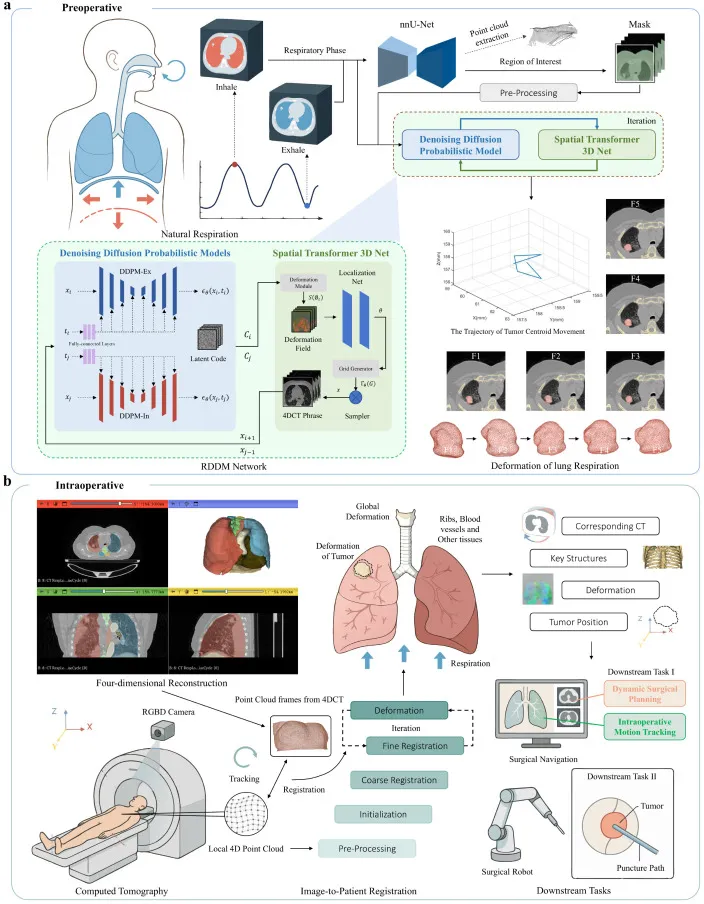
图1. 我们提出的配准框架概述。(a) 吸气末和呼气末阶段的输入LDCT图像用于生成具有一致解剖纹理的4DCT序列。(b) 术中鲁棒的非刚性图像-患者配准实现了无接触动态胸腔肿瘤定位并支持下游临床任务。
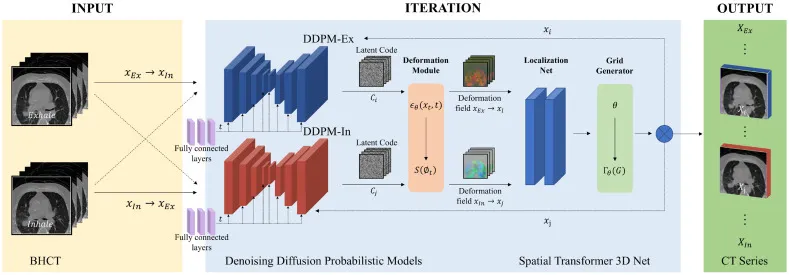
图2. 用于4DCT重建的RDDM网络架构和详细流程。为保证解剖学一致性,中间帧从吸气相和呼气相同时迭代生成。
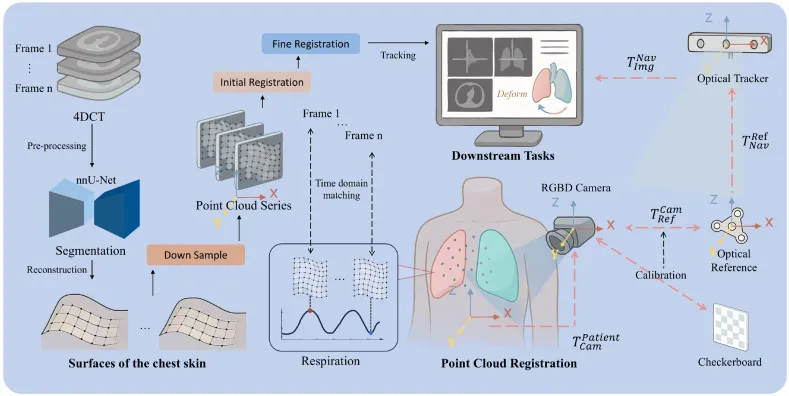
图3. 4DCT图像-患者配准原理及坐标变换。图中黑色箭头所示的左侧部分阐述了配准原理和数据流。橙色箭头所示的右侧部分展示了过程中涉及的矩阵变换。
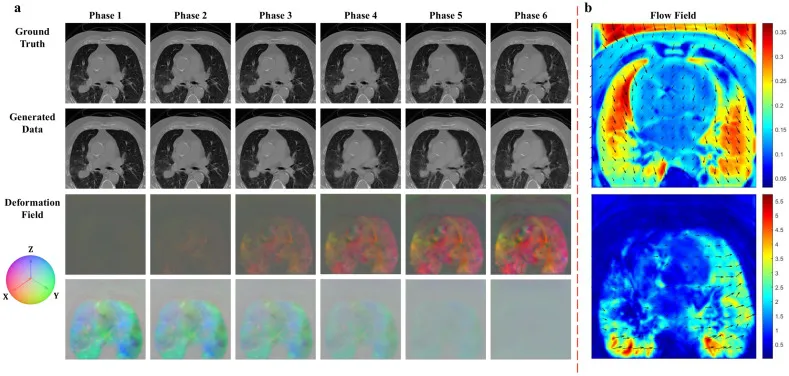
图4. RDDM网络为代表性临床病例生成的4DCT。(a) RDDM网络生成的图像质量定性评估。从上到下:真实值、生成的4DCT序列以及描绘胸腔扩张和收缩的变形场,其中空间维度x、y和z分别映射到红色、绿色和蓝色通道。阶段1到6表示从呼气末到吸气末的进展。(b) RDDM网络生成的图像质量定量分析。从上到下显示了呼气末和吸气末的变形矢量场。
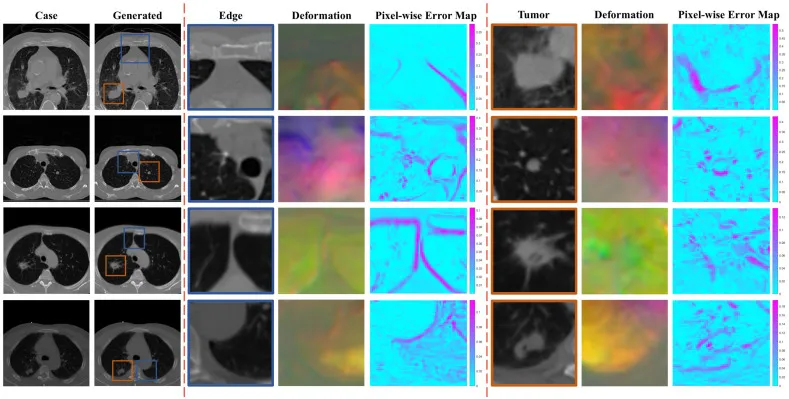
图5. 四个代表性病例中生成的4DCT的纹理细节。前两个病例来自内部数据集,后两个病例来自外部数据集。每个病例显示:真实值、生成的CT、肺边界或肿瘤区域的放大视图、变形场以及相对于真实值的像素级误差热图。变形场使用与图4相同的RGB颜色映射进行可视化,表示胸腔扩张。
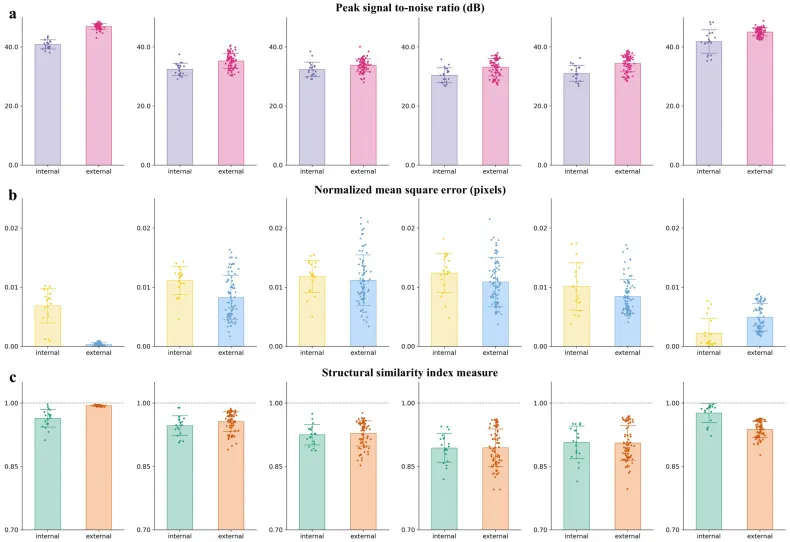
图6. RDDM网络4DCT生成的定量评估。(a) 六个呼吸相的峰值信噪比(PSNR,dB)。(b) 六个呼吸相的归一化均方误差(NMSE,像素)。© 六个呼吸相的结构相似性指数(SSIM)。
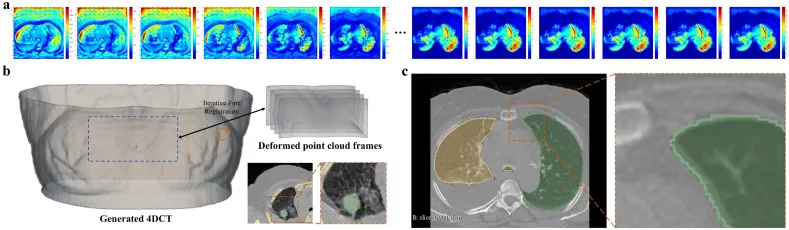
图7. 来自公共4DCT数据集的代表性病例的配准结果。(a) RDDM网络在自然呼吸下生成的多帧4DCT序列(变形场朝向吸气末期)。(b) 将4DCT体积与局部皮肤点云对齐的原理。© 配准后的详细肺部轮廓。
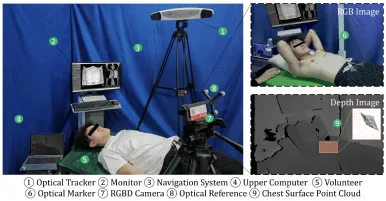
图8. 志愿者试验的实验设置和数据采集。左图显示了实验设置,右图从上到下分别显示了RGB-D相机捕获的RGB图像和深度图像。